骨质疏松症是一种由局部或全身代谢异常引起的慢性疾病,伴有骨量、骨密度下降和骨微结构破坏,最常见于绝经后妇女以及中老年人。铁是人体必需的微量元素,但当体内的铁含量超过转铁蛋白的结合能力时,游离铁的蓄积会在体内造成铁过载环境。在铁过载环境中,骨组织中产生大量活性氧,氧化应激损伤的风险大大增加,成骨细胞的增殖和分化受到抑制。此外,细胞内铁含量的增加会促进破骨细胞对骨的吸收,最终破坏骨代谢的平衡,从而引发骨质疏松症。越来越多的证据表明,铁过载是骨质疏松症的主要诱因。骨质疏松症会给患者带来不同程度的慢性疼痛,也会给骨科植入手术带来一定的困难。在骨质疏松症存在的情况下,由于患者体内成骨细胞的数量减少、质量下降以及广泛存在的慢性炎症,使现有商用骨替代材料的骨修复失败率大大增加。
针对以上问题,张梅教授、王贵宾教授联合bv伟德国际体育第一医院骨科中心-创伤骨科,设计并研发了一种碳纤维增强聚醚醚酮基(CF/PEEK)复合材料植入物的智能表面,该表面可根据患者自身情况定制骨修复进程,植入后自主实现多重内源性调节。智能超分子修饰策略利用具有三吡啶官能团的单体和N-羟乙基丙烯酰胺,通过原位可逆加成-断裂链转移(RAFT)聚合反应在CF/PEEK复合材料植入物表面构建智能超分子层。随后,在分子末端修饰赖氨酸-精氨酸-丝氨酸-精氨酸(KRSR)的小分子肽,最后将阿仑膦酸盐(ALN)接枝到分子链上。植入后,植入物表面刷状大分子最初抵抗巨噬细胞黏附,从而降低免疫炎症的水平。随后,由于铁过载引起的Fe(III)介导的超分子自组装,分子链发生构象变化并转化为机械信号,通过分子末端的 KRSR 短肽的结合能力特异性地传递到成骨前体细胞,通过 YAP/β-catenin 信号轴诱导其向成骨方向分化。此外,成骨细胞分泌碱性磷酸酶(ALP),该酶具有水解磷酸酯键的功能,使ALN释放,这一过程进一步改善了局部骨质疏松微环境。
体外实验在铁过载培养基中进行,证明智能超分子表面具有高度智能的内源性响应能力,且成功实现抑制巨噬细胞黏附、促进成骨细胞分化的效果;为验证该智能超分子表面的体内骨修复能力,构建了铁过载引起的骨质疏松大耳白兔股骨缺损模型,将修饰后的植入材料植入缺损部位,对术后4周和8周的动物进行成骨效果评价,证实了植入物表面内源性调节的成功发生,并有效提升了新骨生成质量,修饰后的植入物周围骨小梁厚度(Tb.Th)和骨体积分数(BV/TV)均有明显提升。
综上,该工作设计了一种具有多重内源性响应能力的智能超分子植入物修饰策略。实验证明,该策略显著增强了铁过载引起的骨质疏松症下的骨缺损修复能力,并改善了种植体周围的病理微环境,为骨质疏松症患者的骨修复提供了一条新的有效途径。相关研究成果近日以“Intelligent Supramolecular Modification for Implants: Endogenous Regulation of Bone Defect Repair in Osteoporosis”为题发表在Advanced Materials期刊上。

图1.智能超分子修饰植入物表面自组装能力验证
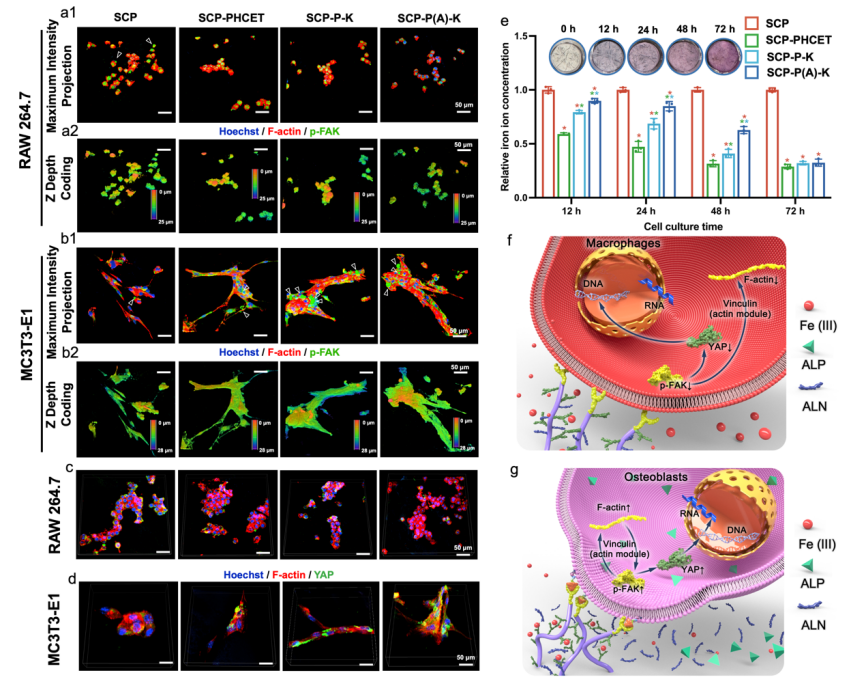
图2. 智能超分子修饰植入物表面对成骨细胞和巨噬细胞的机械效应
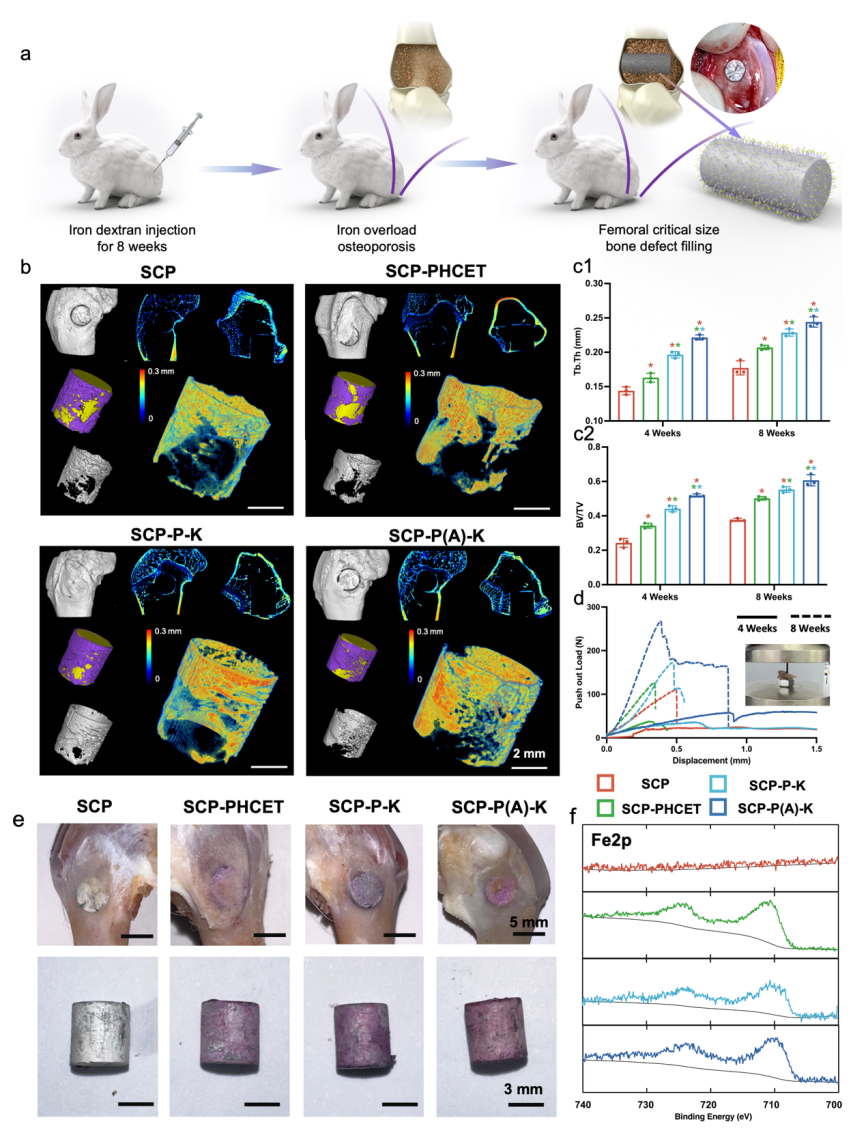
图3. 铁过载引起的骨质疏松症环境下的骨缺损修复评价